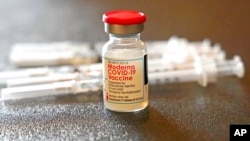
La compañía farmacéutica estadounidense Moderna dijo el miércoles que los estudios provisionales que realizó indicaron que su vacuna contra el COVID-19 es segura y efectiva para niños muy pequeños, y que está presentando una solicitud para su aprobación a los reguladores de medicamentos estadounidenses e internacionales.
En un comunicado publicado en su sitio web, Moderna dijo que los datos provisionales de su estudio de fase 2/3 mostraron "una respuesta robusta de anticuerpos neutralizantes" de una serie de dos dosis de 25 microgramos de su vacuna entre niños de 6 meses a poco menos de 2 años, y niños desde 2 años hasta poco menos de 6.
Con base en estos resultados, la compañía adelantó que presentará una solicitud de aprobación para la serie de dos dosis para niños de 6 meses a poco menos de 6 años a la Administración de Alimentos y Medicamentos de EE. UU., la Agencia Europea de Medicamentos y otros reguladores globales en las próximas semanas.
Si se aprueba, sería la primera vacuna disponible en Estados Unidos para niños menores de 5 años. La vacuna Pfizer-BioNTech actualmente está disponible en dosis más pequeñas para niños de 5 a 12 años y en dosis completas para niños de 12 años en adelante.
Una prueba inicial de la vacuna de Pfizer para niños de 2 a 4 años mostró una respuesta inmunitaria más débil que en adultos, lo que obligó a extender la prueba para probar una tercera dosis. Los resultados se esperan para abril.
* Con información de AP, Reuters y AFP.
¡Conéctate con la Voz de América! Suscríbete a nuestro canal de YouTubey activa las notificaciones, o bien, síguenos en las redes sociales: Facebook, Twitter e Instagram